掲載11 腸内細菌のコントロール(3):〜うんちをもらって病気を治す?〜
これまで、腸内細菌のコントロール方法の1つとして、腸内細菌そのものを摂取するプロバイオティクスを紹介しました。健康な人と病気の人では、腸内細菌のバランスが異なることに着目し、「健康な人の腸内細菌を病気の人に移しかえたら、病気が治るのでは?」と考え、開発された治療方法があります。それが、Fecal Microbiota Transplantation (FMT)と呼ばれる治療法で、健常な人の便(=腸内細菌)を移植することから、「糞便移植療法」と訳されています。今回はこのFMTに関する歴史と最新の知見を紹介したいと思います。
1. ディフィシル症に対するFMT
ディフィシル症はその名が示す通り、Clostridium difficileを原因菌とする感染症です。下痢や発熱を特徴とし、主に抗菌薬治療で腸内細菌叢が撹乱されることでおこります。「抗菌薬でC. difficileもやっつけられるのでは?」と疑問に思うかもしれませんが、C.difficileは多くの抗菌薬に対する耐性をもっています。またClostridium属菌は外からの攻撃にあうと、「芽胞」とよばれる鎧を形成し、休眠状態に入ることで難を逃れようとします。そのため抗菌剤で死滅させるのが難しく、抗菌薬で先に他の菌の増殖が抑えられたところで、その空いたスペースを利用し自らを増殖させていきます。ディフィシル症に対しては、多剤耐性菌にも使われる強力な抗生物質の「バンコマイシン」が使用されますが、治療成績はそこまで芳しくなく、3割程度の人は再発してしまいます。そもそも抗生剤により腸内細菌叢が撹乱されることが発症原因のため、またそこで別の抗生剤を使って治すというのも難しい現状です。
そこで、健常な人の便をディフィシル症の患者に移植して、撹乱された腸内細菌叢を原因から治そうという試みがなされたのが、FMTのはじまりでした。現在まで世界のさまざまな医療機関で試されていますが、FMTのディフィシル症に対する治療効果は極めて良く、再発なしで良好な経過をたどる割合(奏功率)が平均して9割を超えるものとなっています。これらの試験結果は主に海外のものですが、既存の方法に比べて治療効果が非常に高いことから、日本でも再発性のディフィシル症に対するFMT治療が2020年に先進医療として認可され、保険収載を目指した動きがはじまっています。
[参考文献]
1. Gupta K et al. Cureus, 2022
2. 潰瘍性大腸炎に対するFMT
ディフィシル症に対して好成績をおさめているFMTですが、腸内細菌叢の撹乱が原因の病気に対して効果が期待されることから、潰瘍性大腸炎に対する応用も進められています。海外の実施例もいくつかありますが、日本では順天堂大学の石川博士らのA-FMT治療が好成績を示しています。Aはantibiotics(抗生物質)の意味をもち、FMT前にアモキシシリン、ホスホマイシン、メトロニダゾールという性質の異なる3種類の抗生物質を投与して、腸内細菌をリセットする方法です。日本では、別の医療機関で潰瘍性大腸炎に対するFMTが行われていたものの、治療成績が芳しくなく、治療から撤退していた過去がありました。石川博士らは、すでに菌叢の撹乱が起こっている腸内に正常な菌を移植しようとしても、先住者の細菌達が優勢となってしまい、移植した菌が定着しないと考えました。そこで、この先住者達を一掃し、効率的な腸内細菌の移植を促す目的で、抗生物質を事前投与するという方法を行っています。A-FMT療法は従来のFMT療法に比べて高い治療効果が得られていますが、すべてのレシピエント(FMTを受ける人)で効果があるわけではなく、興味深いことにドナーとレシピエントが兄弟であることや、年齢差が近い場合に、長期間にわたり移植された菌叢が安定し、寛解維持効果が高いことがわかっています。臓器移植の場合は免疫拒絶の関係から、HLA(ヒト白血球抗原)の型が近い肉親のほうがマッチするケースが多いですが、腸内細菌叢でも肉親のほうがマッチするというのが驚きです。今後本現象を説明できるような詳細なメカニズムの解明が待たれます。
[参考文献]
1. Zhang X et al. Front Med, 2022
2. Ishikawa D et al. Inflamm Bowel Dis, 2017
3. FMTがメタボにも影響する!?
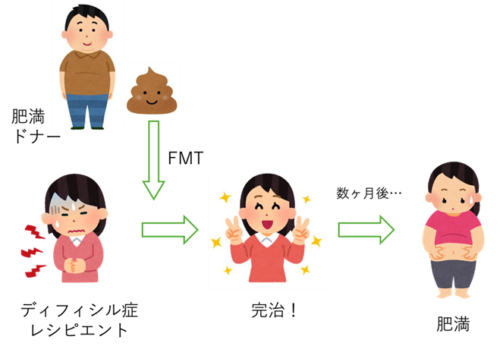
ディフィシル症に対するFMT治療の中で、興味深い知見が副産物として得られています。2015年の米国の症例ですが、ディフィシル症の治療のためにFMTを行った際、便を提供するドナーに肥満傾向があった場合、移植を受けた人が病気は治ったものの、太り始めてしまったというものです。他にも2012年のオランダの研究で、やせ型の人の便を肥満の人に移植したところ、インスリン抵抗性の改善が認められたという報告があります。以前紹介した通り、腸内細菌叢とメタボについては実験動物で十分なエビデンスが得られていることから、上記の結果と統合すると、ヒトでも腸内細菌が代謝性疾患に強く関わっており、腸内細菌をコントロールすることでメタボもコントロールできることがわかります。つい最近、摂取した脂が便から出てくるヤセ薬が薬局でも購入できるようになり大注目されていますが、メタボリックシンドローム対策を求める声が非常に多いことから、そう遠くない未来FMTによるメタボ対策が実用化してくるかもしれません(ただ痩せるためにウンチを飲みますか?と実際に問われた場合、まずは食生活を見直して運動して、それでもダメならといった具合にしたい人も多いかもです)。
[参考文献]
1. Alang N et al. Open Forum Infect Dis, 2015
2. Vrieze A et al. Gastroenterol, 2012
上記以外にも、FMTが抗がん剤(免疫チェックポイント阻害剤)の効果を増強することや、アレルギー症状を改善するという報告もあり、今後さまざまな疾患への応用が期待されています。さらに、良質な菌叢をもつドナー便を集めておく「便バンク」が米国で実装化に向けて進んでおり、日本でもそう遠くない未来「献血」ならぬ「献便(検便ではない)」が一般化するかもしれません。